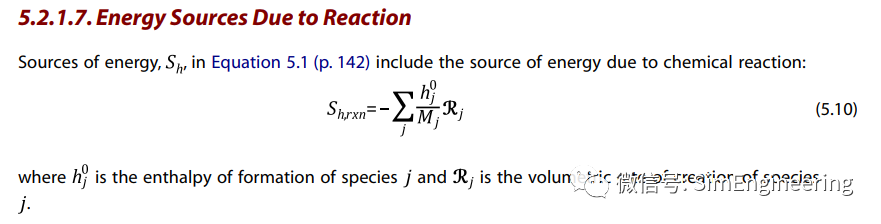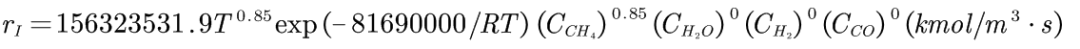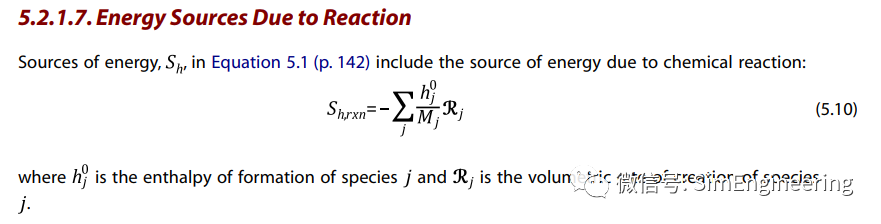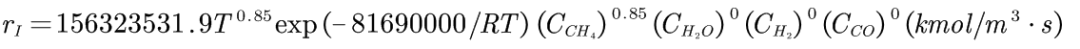反应速率的UDF实现与软件自带结果对比(三)
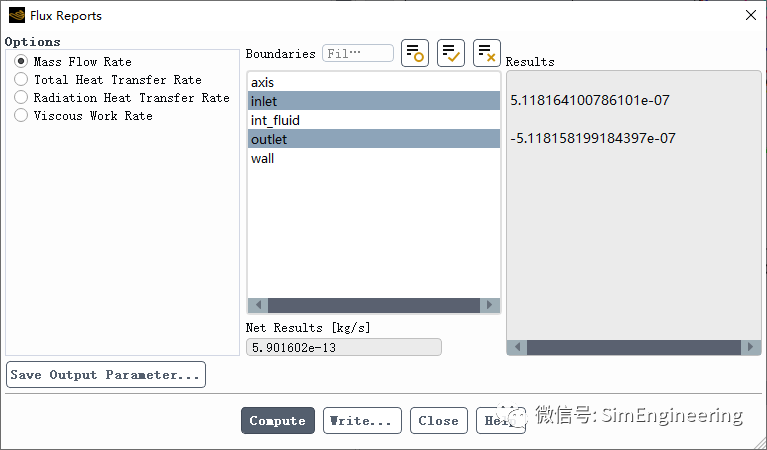
前期推送了多个关于燃烧和化学反应的案例,从应用范围来讲,通用有限速率模型适应更多的应用场景。比如在氢能行业,关于燃料电池电化学的模拟、关于重整制氢的模拟等等,就需要考虑详细的化学反应。因此,我们觉得有必要对详细化学反应的模拟做一些更深入的探讨,接下来我们以一个具体的例子,上一个案例研究了FLUENT的DEFINE_VR_RATE宏求解详细化学反应的关键内容,今天用一个更底层的UDF来求解这个问题。我们考虑以下的化学反应,这是甲烷蒸汽重整制氢的反应之一,反应焓等于摩尔加权的反应物和生成物的生成焓之差,本反应的反应焓为正直,说明是一个吸热反应。FLUENT材料物性的标准状态焓就是材料的生成焓,单位为J/kmol,因此本反应的反应焓转化为FLUENT的反应焓就是206.3×106J/kmol。这个反应的字面理解就是每消耗1kmol的CH4或者每消耗1kmol的H2O或者每生成1kmol的CO或者每生成3kmol的H2,需要吸收206.3×106J的能量。当然,也可以理解为每消耗1/3kmol的CH4或者每消耗1/3kmol的H2O或者每生成1/3kmol的CO或者每生成1kmol的H2,需要吸收1/3×206.3×106J的能量,也即是前文所述的反应焓是摩尔加权计算结果,注意数值上一定要对应。通用有限速率模型中,FLUENT通过在能量方程中增加由于化学反应产生的源项来计算反应热,式5.10中各项的单位为Sh,rxn:W/m3,hj:J/kmol、Mj:kg/kmol、Rj:kg/m3s。该式也等效于ΔH(J/kmol)×R(kmol/m3s)。我们假定反应速率如下,反应速率式的各个变量、各个指数的单位与FLUENT的单位吻合。另外,根据反应式,我们可以得出各个组分的摩尔速率关系为:rCH4=rH2O=rCO=rI,rH2=3rI。也就是各组分摩尔速率之比就等于化学计量数之比,这是化学反应基本常识。在化学反应实验中,通常是得出某个物质的反应速率,也就得到了整个反应以及其他物质的反应速率。FLUENT通过反应摩尔速率式乘以各反应组分的化学计量数,等到该组分的反应摩尔速率,注意反应物的速率为负(表示消耗)、生成物的速率为正(表示生成)。详细化学反应问题本质上其实是在组分输运方程中加入质量源项(反应速率),在能量方程中加入能量源项(反应热)来求解。因此,我们可以通过编写这个源项UDF,然后在相关的方程中加载就可以模拟反应问题了,而无需开启化学反应模型。我们设定反应入口的组分为H2O和CH4,并且摩尔比重为0.6和0.4。其他的相关设置我们就不再细说了,读者朋友可以参考以前的案例。这里需要指出的是,为了能够顺利自启动反应,我们给反应入口设定一个高的温度773.15K。首先,检查一下质量守恒情况,进出口满足质量守恒,这是最基础的,没有这个平衡,整个模拟计算可执行一票否决。然后,我们看一下进出口的各组分的质量分数,和上一个案例FLUENT自身计算的几乎一样。最后,检查一下能量守恒情况。反应热-2.45W,和上一个案例FLUENT自身计算的几乎一样。进出口温度和壁面温度以及温度云图如下,和上一个案例FLUENT自身计算的几乎一样。 著作权归作者所有,欢迎分享,未经许可,不得转载
首次发布时间:2024-02-25
最近编辑:9月前